- Mensajes: 34
- Gracias recibidas: 13
Caso clínico Universidad El Bosque
- Webmaster
- [Webmaster]
-
 Autor del tema
Autor del tema
- Fuera de línea
- Administrador
-

Menos
Más
3 años 10 meses antes - 3 años 10 meses antes #53
por Webmaster
Caso clínico Universidad El Bosque Publicado por Webmaster
Mujer de 39 años sin antecedentes de importancia. Abogada, lateralidad diestra, la última vez que fue vista bien fue el 13/03/2022 a las 23:00, en ese momento, inicia con cefalea y dolor ocular izquierdo progresivos. A medianoche, la paciente desarrolla hemiparesia izquierda. Acude de inmediato a un hospital en Arauca donde a la evaluación de funciones neurológicas, la califican con un National Institute of Health Stroke Scale (NIHSS) de 18 y le toman una tomografía axial computarizada (TAC) de cráneo simple. Se desconoce la hora que dicha neuroimagen fue realizada. Los hallazgos evidenciaron una arteria cerebral media (ACM) derecha hiperdensa, confirmando un ACV isquémico de características agudas. Como parte de los estudios imagenológicos, se realiza un Doppler de vasos del cuello y se documenta una estenosis del 97% de la arteria carótida interna derecha. Lastimosamente, no se hacen terapias de reperfusión en ese momento, las razones no están documentadas.
El siguiente día, 14/03/2022 a las 10:17 desde de la unidad de cuidados intensivos (UCI) del hospital en Arauca se hace la solicitud de remisión a un hospital de mayor complejidad con diagnóstico de “ataque cerebrovascular isquémico” para “realización de endarterectomía”. Es aceptada por nuestra institución en Bogotá a las 14:00 e ingresa a urgencias en traslado secundario a las 22:00 de ese mismo día.
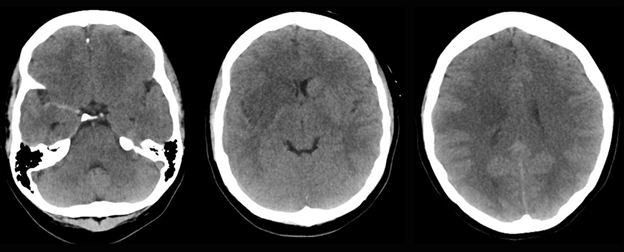
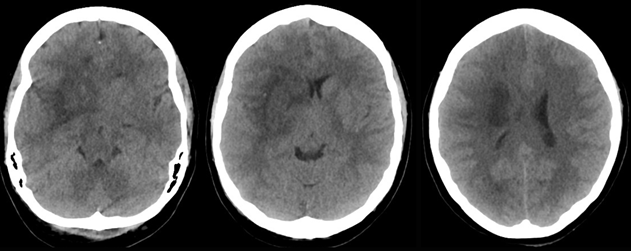
Al ingreso, la paciente no tenía hallazgos a la revisión por sistemas relevantes. Los signos vitales de ingreso y el examen general fueron normales. El NIHSS de ingreso fue 18 (1A:1, 1B:0, 1C:0, 2:1, 3:2, 4:2, 5A:1, 5B:4, 6A:0, 6B:4, 7:0, 8:1, 9:0, 10:1, 11:1). Es llevada a TAC de cráneo simple el 14/03/22 a las 22:32, el cual evidencia una ACM hiperdensa, con un ASPECTS de 4, se encontró compromiso de la ínsula, el núcleo caudado, el núcleo lenticular, la cápsula interna, el territorio de la ACM, en su porción de M4 y M5 (Ver Imagen 1).
Imagen 1
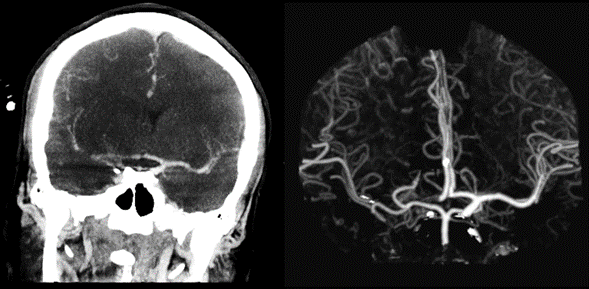
En el AngioTAC de vasos de cuello y cerebro, se evidencia la oclusión de la carótida interna derecha desde el tercio proximal, con oclusión de segmentos M1 y M2 y de la ACA en segmento A1 derechos. La colateralidad estaba preservada en aproximadamente 50% (Imagen 2).
Imagen 2
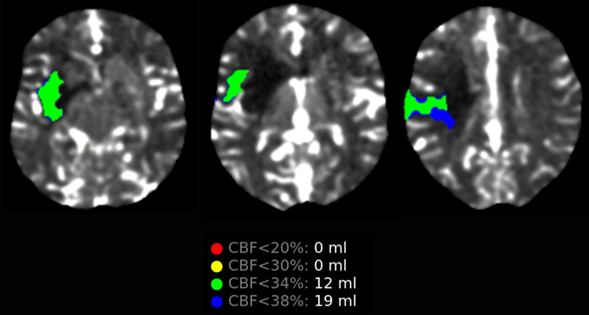
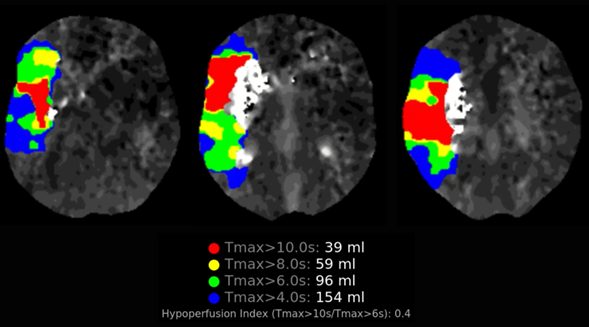
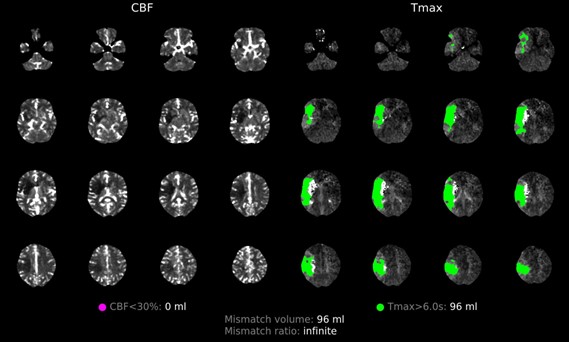
Aunque el ASPECTS era bajo, los cambios en la tomografía se consideraron sutiles para el tiempo de evolución del cuadro y el NIHSS. Se decide realizar perfusión por TAC cerebral con análisis automatizado (RAPIDai) para evaluar los territorios de penumbra y de necrosis de la paciente. Este algoritmo mostró un área de necrosis (CBF<30%) de 0 mL, sin embargo está infravalorado debido a que ya hay una hipodensidad instaurada. Aparte de la hipodensidad no hay más territorios infartados (Imagen 3a). El área de penumbra calculado (Tmax>6 segs) fue calculada en 96 mL de tejido cerebral (Imagen 3b). El consolidado de imágenes por perfusión muestra un mismatch de penumbra/necrosis de 96 mL con un radio infinito debido a que la hipodensidad no se calcula en RAPIDai como necrosis (Imagen 3c).
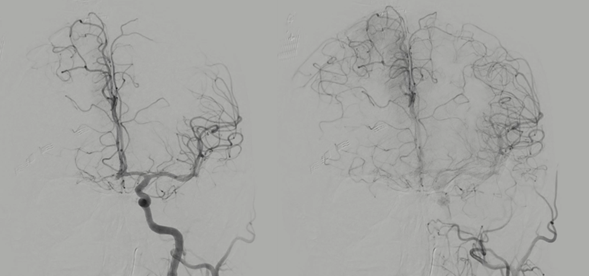
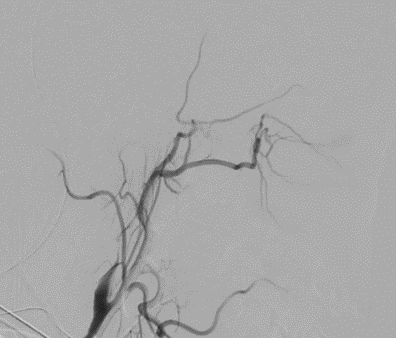
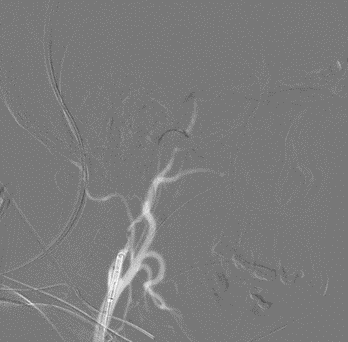
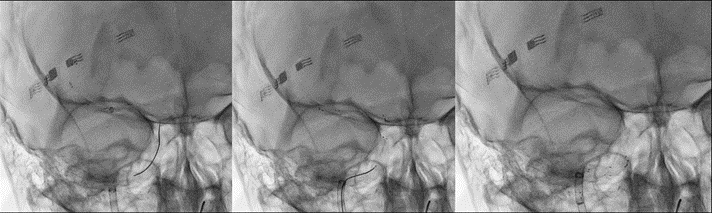
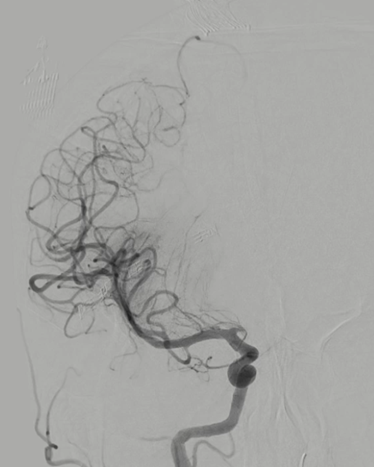
La paciente se consideró candidata a trombectomía mecánica teniendo en cuenta que tenía una gran cantidad de penumbra. En la angiografía se ve cómo hay una muy buena colateralidad a territorios de la arteria cerebral anterior (ACA) e incluso ACM derechas desde territorio de carótida interna izquierda (Imagen 4a). En la angiografía de la carótida derecha, podemos visualizar una disección de la ACI en su porción proximal (Imagen 4b). Esta fue franqueada mediante aspiración de trombo y colocación de un stent en este lugar (Imagen 4c).
Imagen 4a
Imagen 4b
Imagen 4c
Posteriormente se hizo trombectomía en ACM derecha, mediante técnica combinada Solitaire y aspiración (Imagen 5), para conseguir finalmente una reperfusión TICI 2b (Imagen 6). La punción femoral fue a las 07:11 y la hora de reperfusión cerebral fue a las 07:41 del 15/03/2022.
Imagen 5
Imagen 6
Durante los cuidados post trombectomía y durante su estancia en UCI, la paciente sufrió una sepsis de origen pulmonar y requirió intubación endotraqueal por aproximadamente una semana. Las imágenes de control mostraron un aumento discreto del tamaño del infarto comparado a las imágenes de ingreso comprometiendo principalmente el territorio ganglio basal y la ínsula del lado derecho. El infarto no creció, no presentó transformación hemorrágica, ni comprometió la totalidad de la penumbra evidenciada en la perfusión cerebral. Mostramos una imagen de control 10 días post trombectomía (Imagen 7).
Imagen 7
La paciente en su control a los 30 días post ACV se encontraba mucho mejor, con un NIHSS de 8 y un mRS de 4 (complicado por una fractura reciente de peroné izquierdo que limita la marcha). Ya la paciente estaba iniciando marcha con ayuda. La prevención secundaria se hizo con doble antiagregación (ASA + clopidogrel) y estatina de alta intensidad. La etiología del ACV fue por disección carotídea, sin embargo, la causa de la disección nunca se aclaró.
El 28/06/2022 contactamos nuevamente a la paciente. Manifestó que todavía persiste con dificultades para movilizarse dentro de su casa y poca asistencia para sus actividades básicas, el mRS calculado para este momento fue de 4. Sin embargo, la paciente refiere tener una buena calidad de vida, con bienestar físico y psicosocial, está muy optimista con el proceso de rehabilitación.
Discusión:
Los estudios DEFUSE 3 y DAWN demostraron la efectividad de la trombectomía en ACV isquémico en ventanas extendidas de 16 y 24 horas respectivamente. Estos estudios ofrecieron trombectomía a pacientes con evidencia de mismatch clínico-radiológico o con evidencia de penumbra significativa. Estos hallazgos se confirmaron mediante la toma de una resonancia o imágenes por perfusión, con cuantificación automatizada de los respectivos volúmenes (1, 2).
Presentamos este caso dado que es una experiencia de trombectomía en ventana muy extendida, con una reperfusión casi de 28 horas post inicio de síntomas. Esto es, significativamente más allá de lo que se ha validado en estudios aleatorizados disponibles al momento, por ende, no está incluido en las guías de práctica clínica. Esta paciente se consideró candidata a trombectomía debido a que es una paciente muy joven, con buena colateralidad, un área isquémica de tamaño moderado, pero con una penumbra muy grande, de prácticamente toda la circulación anterior, y con una razón de intensidad de hipoperfusión favorable (HIR <0.5) que predice una tasa de crecimiento del infarto lenta. En el caso de que la paciente no fuera intervenida, es altamente probable que hubiera quedado con una discapacidad muy severa, tal vez hubiera requerido de craniectomía descompresiva y el riesgo de mortalidad asociada al evento o a complicaciones sería significativo.
En la literatura hay algunos reportes provenientes de estudios observacionales mostrando la eficacia y seguridad de la trombectomía en el ACV isquémico de más de 24 horas de evolución (3, 4). Típicamente estos casos son pacientes muy seleccionados que se determinan como “progresores lentos”, ya que logran mantener viable el tejido isquémico por tiempos muy prolongados. Estos pacientes presentan mejores desenlaces con la reperfusión comparados con los progresores más rápidos (5, 6).
Este caso es un recordatorio que el paradigma del tiempo en ACV debe ser reevaluado cada día, ya que cada vez más tenemos literatura médica con evidencia clínica que hace énfasis en concentrarnos en el paradigma de tejido. Aunque las guías son increíblemente valiosas, cada caso se debe individualizar y en ocasiones hay que pensar más allá de ellas para ofrecerle el mejor tratamiento posible a nuestros pacientes. Por último, herramientas avanzadas como la perfusión y la cuantificación automática de imágenes no están disponibles en muchos lugares, lo que limita estas conductas. Sin embargo, estas imágenes pueden no ser absolutamente necesarias para definir a los pacientes y la tendencia actual de la investigación en ACV es volver a estudios imagenológicos básicos en las ventanas extendidas (7, .
.
Bibliografía
1. Albers, G. W., Marks, M. P., Kemp, S., Christensen, S., Tsai, J. P., Ortega-Gutierrez, S., McTaggart, R. A., Torbey, M. T., Kim-Tenser, M., Leslie-Mazwi, T., Sarraj, A., Kasner, S. E., Ansari, S. A., Yeatts, S. D., Hamilton, S., Mlynash, M., Heit, J. J., Zaharchuk, G., Kim, S., … Lansberg, M. G. (2018). Thrombectomy for stroke at 6 to 16 hours with selection by perfusion imaging. New England Journal of Medicine, 378( , 708–718.
doi.org/10.1056/nejmoa1713973
, 708–718.
doi.org/10.1056/nejmoa1713973
2. Nogueira, R. G., Jadhav, A. P., Haussen, D. C., Bonafe, A., Budzik, R. F., Bhuva, P., Yavagal, D. R., Ribo, M., Cognard, C., Hanel, R. A., Sila, C. A., Hassan, A. E., Millan, M., Levy, E. I., Mitchell, P., Chen, M., English, J. D., Shah, Q. A., Silver, F. L., … Jovin, T. G. (2018). Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. New England Journal of Medicine, 378(1), 11–21. doi.org/10.1056/nejmoa1706442
3. Desai, S. M., Haussen, D. C., Aghaebrahim, A., Al-Bayati, A. R., Santos, R., Nogueira, R. G., Jovin, T. G., & Jadhav, A. P. (2018). Thrombectomy 24 hours after stroke: Beyond dawn. Journal of NeuroInterventional Surgery, 10(11), 1039–1042. doi.org/10.1136/neurintsurg-2018-013923
4. Manning, N. W., Wenderoth, J., Alsahli, K., Cordato, D., Cappelen-Smith, C., McDougall, A., Zagami, A. S., & Cheung, A. (2018). Endovascular thrombectomy >24-hr from stroke symptom onset. Frontiers in Neurology, 9. doi.org/10.3389/fneur.2018.00501
5. Rocha, M., & Jovin, T. G. (2017). Fast versus slow progressors of infarct growth in large vessel occlusion stroke. Stroke, 48(9), 2621–2627. doi.org/10.1161/strokeaha.117.017673
6. Albers, G. W. (2018). Late window paradox. Stroke, 49(3), 768–771. doi.org/10.1161/strokeaha.117.020200
7. Almekhlafi, M. A., Kunz, W. G., McTaggart, R. A., Jayaraman, M. V., Najm, M., Ahn, S. H., Fainardi, E., Rubiera, M., Khaw, A. V., Zini, A., Hill, M. D., Demchuk, A. M., Goyal, M., & Menon, B. K. (2019). Imaging triage of patients with late-window (6–24 hours) acute ischemic stroke: A comparative study using multiphase CT angiography versus CT Perfusion. American Journal of Neuroradiology, 41(1), 129–133. doi.org/10.3174/ajnr.a6327
8. Nogueira, R. G., Jadhav, A. P., Haussen, D. C., Bonafe, A., Budzik, R. F., Bhuva, P., Yavagal, D. R., Ribo, M., Cognard, C., Hanel, R. A., Sila, C. A., Hassan, A. E., Millan, M., Levy, E. I., Mitchell, P., Chen, M., English, J. D., Shah, Q. A., Silver, F. L., … Jovin, T. G. (2018). Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. New England Journal of Medicine, 378(1), 11–21. doi.org/10.1056/nejmoa1706442
El siguiente día, 14/03/2022 a las 10:17 desde de la unidad de cuidados intensivos (UCI) del hospital en Arauca se hace la solicitud de remisión a un hospital de mayor complejidad con diagnóstico de “ataque cerebrovascular isquémico” para “realización de endarterectomía”. Es aceptada por nuestra institución en Bogotá a las 14:00 e ingresa a urgencias en traslado secundario a las 22:00 de ese mismo día.
Al ingreso, la paciente no tenía hallazgos a la revisión por sistemas relevantes. Los signos vitales de ingreso y el examen general fueron normales. El NIHSS de ingreso fue 18 (1A:1, 1B:0, 1C:0, 2:1, 3:2, 4:2, 5A:1, 5B:4, 6A:0, 6B:4, 7:0, 8:1, 9:0, 10:1, 11:1). Es llevada a TAC de cráneo simple el 14/03/22 a las 22:32, el cual evidencia una ACM hiperdensa, con un ASPECTS de 4, se encontró compromiso de la ínsula, el núcleo caudado, el núcleo lenticular, la cápsula interna, el territorio de la ACM, en su porción de M4 y M5 (Ver Imagen 1).
Imagen 1
En el AngioTAC de vasos de cuello y cerebro, se evidencia la oclusión de la carótida interna derecha desde el tercio proximal, con oclusión de segmentos M1 y M2 y de la ACA en segmento A1 derechos. La colateralidad estaba preservada en aproximadamente 50% (Imagen 2).
Imagen 2
Aunque el ASPECTS era bajo, los cambios en la tomografía se consideraron sutiles para el tiempo de evolución del cuadro y el NIHSS. Se decide realizar perfusión por TAC cerebral con análisis automatizado (RAPIDai) para evaluar los territorios de penumbra y de necrosis de la paciente. Este algoritmo mostró un área de necrosis (CBF<30%) de 0 mL, sin embargo está infravalorado debido a que ya hay una hipodensidad instaurada. Aparte de la hipodensidad no hay más territorios infartados (Imagen 3a). El área de penumbra calculado (Tmax>6 segs) fue calculada en 96 mL de tejido cerebral (Imagen 3b). El consolidado de imágenes por perfusión muestra un mismatch de penumbra/necrosis de 96 mL con un radio infinito debido a que la hipodensidad no se calcula en RAPIDai como necrosis (Imagen 3c).
La paciente se consideró candidata a trombectomía mecánica teniendo en cuenta que tenía una gran cantidad de penumbra. En la angiografía se ve cómo hay una muy buena colateralidad a territorios de la arteria cerebral anterior (ACA) e incluso ACM derechas desde territorio de carótida interna izquierda (Imagen 4a). En la angiografía de la carótida derecha, podemos visualizar una disección de la ACI en su porción proximal (Imagen 4b). Esta fue franqueada mediante aspiración de trombo y colocación de un stent en este lugar (Imagen 4c).
Imagen 4a
Imagen 4b
Imagen 4c
Posteriormente se hizo trombectomía en ACM derecha, mediante técnica combinada Solitaire y aspiración (Imagen 5), para conseguir finalmente una reperfusión TICI 2b (Imagen 6). La punción femoral fue a las 07:11 y la hora de reperfusión cerebral fue a las 07:41 del 15/03/2022.
Imagen 5
Imagen 6
Durante los cuidados post trombectomía y durante su estancia en UCI, la paciente sufrió una sepsis de origen pulmonar y requirió intubación endotraqueal por aproximadamente una semana. Las imágenes de control mostraron un aumento discreto del tamaño del infarto comparado a las imágenes de ingreso comprometiendo principalmente el territorio ganglio basal y la ínsula del lado derecho. El infarto no creció, no presentó transformación hemorrágica, ni comprometió la totalidad de la penumbra evidenciada en la perfusión cerebral. Mostramos una imagen de control 10 días post trombectomía (Imagen 7).
Imagen 7
La paciente en su control a los 30 días post ACV se encontraba mucho mejor, con un NIHSS de 8 y un mRS de 4 (complicado por una fractura reciente de peroné izquierdo que limita la marcha). Ya la paciente estaba iniciando marcha con ayuda. La prevención secundaria se hizo con doble antiagregación (ASA + clopidogrel) y estatina de alta intensidad. La etiología del ACV fue por disección carotídea, sin embargo, la causa de la disección nunca se aclaró.
El 28/06/2022 contactamos nuevamente a la paciente. Manifestó que todavía persiste con dificultades para movilizarse dentro de su casa y poca asistencia para sus actividades básicas, el mRS calculado para este momento fue de 4. Sin embargo, la paciente refiere tener una buena calidad de vida, con bienestar físico y psicosocial, está muy optimista con el proceso de rehabilitación.
Discusión:
Los estudios DEFUSE 3 y DAWN demostraron la efectividad de la trombectomía en ACV isquémico en ventanas extendidas de 16 y 24 horas respectivamente. Estos estudios ofrecieron trombectomía a pacientes con evidencia de mismatch clínico-radiológico o con evidencia de penumbra significativa. Estos hallazgos se confirmaron mediante la toma de una resonancia o imágenes por perfusión, con cuantificación automatizada de los respectivos volúmenes (1, 2).
Presentamos este caso dado que es una experiencia de trombectomía en ventana muy extendida, con una reperfusión casi de 28 horas post inicio de síntomas. Esto es, significativamente más allá de lo que se ha validado en estudios aleatorizados disponibles al momento, por ende, no está incluido en las guías de práctica clínica. Esta paciente se consideró candidata a trombectomía debido a que es una paciente muy joven, con buena colateralidad, un área isquémica de tamaño moderado, pero con una penumbra muy grande, de prácticamente toda la circulación anterior, y con una razón de intensidad de hipoperfusión favorable (HIR <0.5) que predice una tasa de crecimiento del infarto lenta. En el caso de que la paciente no fuera intervenida, es altamente probable que hubiera quedado con una discapacidad muy severa, tal vez hubiera requerido de craniectomía descompresiva y el riesgo de mortalidad asociada al evento o a complicaciones sería significativo.
En la literatura hay algunos reportes provenientes de estudios observacionales mostrando la eficacia y seguridad de la trombectomía en el ACV isquémico de más de 24 horas de evolución (3, 4). Típicamente estos casos son pacientes muy seleccionados que se determinan como “progresores lentos”, ya que logran mantener viable el tejido isquémico por tiempos muy prolongados. Estos pacientes presentan mejores desenlaces con la reperfusión comparados con los progresores más rápidos (5, 6).
Este caso es un recordatorio que el paradigma del tiempo en ACV debe ser reevaluado cada día, ya que cada vez más tenemos literatura médica con evidencia clínica que hace énfasis en concentrarnos en el paradigma de tejido. Aunque las guías son increíblemente valiosas, cada caso se debe individualizar y en ocasiones hay que pensar más allá de ellas para ofrecerle el mejor tratamiento posible a nuestros pacientes. Por último, herramientas avanzadas como la perfusión y la cuantificación automática de imágenes no están disponibles en muchos lugares, lo que limita estas conductas. Sin embargo, estas imágenes pueden no ser absolutamente necesarias para definir a los pacientes y la tendencia actual de la investigación en ACV es volver a estudios imagenológicos básicos en las ventanas extendidas (7,
Bibliografía
1. Albers, G. W., Marks, M. P., Kemp, S., Christensen, S., Tsai, J. P., Ortega-Gutierrez, S., McTaggart, R. A., Torbey, M. T., Kim-Tenser, M., Leslie-Mazwi, T., Sarraj, A., Kasner, S. E., Ansari, S. A., Yeatts, S. D., Hamilton, S., Mlynash, M., Heit, J. J., Zaharchuk, G., Kim, S., … Lansberg, M. G. (2018). Thrombectomy for stroke at 6 to 16 hours with selection by perfusion imaging. New England Journal of Medicine, 378(
2. Nogueira, R. G., Jadhav, A. P., Haussen, D. C., Bonafe, A., Budzik, R. F., Bhuva, P., Yavagal, D. R., Ribo, M., Cognard, C., Hanel, R. A., Sila, C. A., Hassan, A. E., Millan, M., Levy, E. I., Mitchell, P., Chen, M., English, J. D., Shah, Q. A., Silver, F. L., … Jovin, T. G. (2018). Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. New England Journal of Medicine, 378(1), 11–21. doi.org/10.1056/nejmoa1706442
3. Desai, S. M., Haussen, D. C., Aghaebrahim, A., Al-Bayati, A. R., Santos, R., Nogueira, R. G., Jovin, T. G., & Jadhav, A. P. (2018). Thrombectomy 24 hours after stroke: Beyond dawn. Journal of NeuroInterventional Surgery, 10(11), 1039–1042. doi.org/10.1136/neurintsurg-2018-013923
4. Manning, N. W., Wenderoth, J., Alsahli, K., Cordato, D., Cappelen-Smith, C., McDougall, A., Zagami, A. S., & Cheung, A. (2018). Endovascular thrombectomy >24-hr from stroke symptom onset. Frontiers in Neurology, 9. doi.org/10.3389/fneur.2018.00501
5. Rocha, M., & Jovin, T. G. (2017). Fast versus slow progressors of infarct growth in large vessel occlusion stroke. Stroke, 48(9), 2621–2627. doi.org/10.1161/strokeaha.117.017673
6. Albers, G. W. (2018). Late window paradox. Stroke, 49(3), 768–771. doi.org/10.1161/strokeaha.117.020200
7. Almekhlafi, M. A., Kunz, W. G., McTaggart, R. A., Jayaraman, M. V., Najm, M., Ahn, S. H., Fainardi, E., Rubiera, M., Khaw, A. V., Zini, A., Hill, M. D., Demchuk, A. M., Goyal, M., & Menon, B. K. (2019). Imaging triage of patients with late-window (6–24 hours) acute ischemic stroke: A comparative study using multiphase CT angiography versus CT Perfusion. American Journal of Neuroradiology, 41(1), 129–133. doi.org/10.3174/ajnr.a6327
8. Nogueira, R. G., Jadhav, A. P., Haussen, D. C., Bonafe, A., Budzik, R. F., Bhuva, P., Yavagal, D. R., Ribo, M., Cognard, C., Hanel, R. A., Sila, C. A., Hassan, A. E., Millan, M., Levy, E. I., Mitchell, P., Chen, M., English, J. D., Shah, Q. A., Silver, F. L., … Jovin, T. G. (2018). Thrombectomy 6 to 24 hours after stroke with a mismatch between deficit and infarct. New England Journal of Medicine, 378(1), 11–21. doi.org/10.1056/nejmoa1706442
Adjuntos:
Última Edición: 3 años 10 meses antes por Webmaster.
Por favor, Identificarse para unirse a la conversación.
Moderadores: Jorge Mario Gaspar Toro, Juan Pablo Ovalle Rojas